es la región del espacio definido por una determinada solución particular, espacial e independiente del tiempo, a la ecuación de Schrödinger para el caso de un electrón sometido a un potencial coulombiano. La elección de tres números cuánticos en la solución general señalan unívocamente a un estado monoelectrónico posible.
Estos tres números cuánticos hacen referencia a la energía total del electrón, el momento angular orbital y la proyección del mismo sobre el eje z del sistema del laboratorio y se denotan por
{\displaystyle \langle {\vec {r}}|nlm\rangle =\psi _{n,l}^{m}({\vec {r}})}
Un orbital también puede representar la posición independiente del tiempo de un electrón en una molécula, en cuyo caso se denomina orbital molecular.
La combinación de todos los orbitales atómicos dan lugar a la corteza electrónica, representada por el modelo de capas, el cual se ajusta a cada elemento químico según la configuración electrónica correspondiente.
Ecuación de Schordinger
ecuación de Schrödinger, desarrollada por el físico austríaco Erwin Schrödinger en 1925, describe la evolución temporal de una partícula subatómica masiva de naturaleza ondulatoria y no relativista. Es de importancia central en la teoría de la mecánica cuántica, donde representa para las partículas microscópicas un papel análogo a la segunda ley de Newton en la mecánica clásica. Las partículas microscópicas incluyen a las partículas elementales, tales como electrones, así como sistemas de partículas, tales como núcleos atómicos.
Principio de Incertidumbre de Heinsenberg
la relación de indeterminación de Heisenberg o principio de incertidumbre establece la imposibilidad de que determinados pares de magnitudes físicas observables y complementarias sean conocidas con precisión arbitraria. Sucintamente, afirma que no se puede determinar, en términos de la física cuántica, simultáneamente y con precisión arbitraria, ciertos pares de variables físicas, como son, la posición y el momento lineal (cantidad de movimiento) de un objeto dado. En otras palabras, cuanta mayor certeza se busca en determinar la posición de una partícula, menos se conoce su cantidad de movimientos lineales y, por tanto, su masa y velocidad. Este principio fue enunciado por Werner Heisenberg en 1925.
El principio de indeterminación no tiene un análogo clásico y define una de las diferencias fundamentales entre física clásica y física cuántica. Desde un punto de vista lógico es una consecuencia de axiomas corrientes de la mecánica cuántica y por tanto estrictamente se deduce de los mismos
Breve descripción sobre la dualidad Onda Partícula
La dualidad onda-corpúsculo, también llamada dualidad onda-partícula, postula que todas las partículas pueden describirse alternativamente aludiendo a su naturaleza ondulatoria. Más específicamente, como partículas pueden presentar interacciones muy localizadas y como ondas exhiben el fenómeno de la interferencia.
De acuerdo con la física clásica existen diferencias entre onda y partícula. Una partícula ocupa un lugar en el espacio y tiene masa mientras que una onda se extiende en el espacio caracterizándose por tener una velocidad definida y masa nula.
Actualmente se considera que la dualidad onda-partícula es un “concepto de la mecánica cuántica según el cual no hay diferencias fundamentales entre partículas y ondas: las partículas pueden comportarse como ondas y viceversa”. (Stephen Hawking, 2001)
Este es un hecho comprobado experimentalmente en múltiples ocasiones. Fue introducido por Louis-Victor de Broglie, físico francés de principios del siglo XX. En 1924 en su tesis doctoral, inspirada en experimentos sobre la difracción de electrones, propuso la existencia de ondas de materia, es decir que toda materia tenía una onda asociada a ella. Esta idea revolucionaria, fundada en la analogía con que la radiación tenía una partícula asociada, propiedad ya demostrada entonces, no despertó gran interés, pese a lo acertado de sus planteamientos, ya que no tenía evidencias de producirse. Sin embargo, Einstein reconoció su importancia y cinco años después, en 1929, De Broglie recibió el Nobel en Física por su trabajo.
Su trabajo decía que la longitud de onda {\displaystyle \lambda } de la onda asociada a la materia era:
{\displaystyle \lambda ={\frac {h}{p}}}
donde {\displaystyle h} es la constante de Planck y {\displaystyle p} es el momento lineal de la partícula de materia.
En general {\displaystyle p=m\gamma v} siendo {\displaystyle v} la velocidad de la partícula, {\displaystyle m} su masa y {\displaystyle \gamma } el factor de Lorentz
Si la velocidad de la partícula es despreciable respecto de la velocidad de la luz, el factor de Lorentz es prácticamente la unidad y el momento lineal se puede calcular mediante la aproximación clásica no relativista {\displaystyle p=mv}
Modelo del Átomo de Bohr
El modelo atómico de Bohr1 o de Bohr-Rutherford es un modelo clásico del átomo, pero fue el primer modelo atómico en el que se introduce una cuantización a partir de ciertos postulados. Dado que la cuantización del momento es introducida en forma ad hoc, el modelo puede considerarse transicional en cuanto a que se ubica entre la mecánica clásica y la cuántica. Fue propuesto en 1913 por el físico danés Niels Bohr,2 para explicar cómo los electrones pueden tener órbitas estables alrededor del núcleo y por qué los átomos presentaban espectros de emisión característicos (dos problemas que eran ignorados en el modelo previo de Rutherford). Además el modelo de Bohr incorporaba ideas tomadas del efecto fotoeléctrico, explicado por Albert Einstein en 1905.
El efecto Fotoeléctrico
La emisión de electrones por metales iluminados con luz de determinada frecuencia fue observada a finales del siglo XIX por Hertz y Hallwachs. El proceso por el cual se liberan electrones de un material por la acción de la radiación se denomina efecto fotoeléctrico o emisión fotoeléctrica. Sus características esenciales son:
Para cada sustancia hay una frecuencia mínima o umbral de la radiación electromagnética por debajo de la cual no se producen fotoelectrones por más intensa que sea la radiación.
La emisión electrónica aumenta cuando se incrementa la intensidad de la radiación que incide sobre la superficie del metal, ya que hay más energía disponible para liberar electrones.
En los metales hay electrones que se mueven más o menos libremente a través de la red cristalina, estos electrones no escapan del metal a temperaturas normales por que no tienen energía suficiente. Calentando el metal es una manera de aumentar su energía. Los electrones "evaporados" se denominan termoelectrones, este es el tipo de emisión que hay en las válvulas electrónicas. Vamos a ver que también se pueden liberar electrones (fotoelectrones) mediante la absorción por el metal de la energía de radiación electromagnética.
El objetivo de la práctica simulada es la determinación de la energía de arranque de los electrones de un metal, y el valor de la constante de Planck. Para ello, disponemos de un conjunto de lámparas que emiten luz de distintas frecuencias y placas de distintos metales que van a ser iluminadas por la luz emitida por esas lámparas especiales.
Descripción
Sea f la energía mínima necesaria para que un electrón escape del metal. Si el electrón absorbe una energía E, la diferencia E-f, será la energía cinética del electrón emitido.
Einstein explicó las características del efecto fotoeléctrico, suponiendo que cada electrón absorbía un cuanto de radiación o fotón. La energía de un fotón se obtiene multiplicando la constante h de Planck por la frecuencia f de la radiación electromagnética.
E=hf
Si la energía del fotón E, es menor que la energía de arranque f, no hay emisión fotoeléctrica. En caso contrario, si hay emisión y el electrón sale del metal con una energía cinética Ek igual a E-f.
Por otra parte, cuando la placa de área S se ilumina con cierta intensidad I, absorbe una energía en la unidad de tiempo proporcional a IS, basta dividir dicha energía entre la cantidad hf para obtener el número de fotones que inciden sobre la placa en la unidad de tiempo. Como cada electrón emitido toma la energía de un único fotón, concluimos que el número de electrones emitidos en la unidad de tiempo es proporcional a la intensidad de la luz que ilumina la placa
Experimento.gif (2763 bytes)
Mediante una fuente de potencial variable, tal como se ve en la figura podemos medir la energía cinética máxima de los electrones emitidos, véase el movimiento de partículas cargadas en un campo eléctrico.
Aplicando una diferencia de potencial V entre las placas A y C se frena el movimiento de los fotoelectrones emitidos. Para un voltaje V0 determinado, el amperímetro no marca el paso de corriente, lo que significa que ni aún los electrones más rápidos llegan a la placa C. En ese momento, la energía potencial de los electrones se hace igual a la energía cinética.
Variando la frecuencia f, (o la longitud de onda de la radiación que ilumina la placa) obtenemos un conjunto de valores del potencial de detención V0. Llevados a un gráfico obtenemos una serie de puntos (potencial de detención, frecuencia) que se aproximan a una línea recta.
La ordenada en el origen mide la energía de arranque en electrón-voltios f/e. Y la pendiente de la recta es h/e. Midiendo el ángulo de dicha pendiente y usando el valor de la carga del electrón e= 1.6 10-19 C, obtendremos el valor de la constante de Planck, h=6.63 10-34 Js.
Resultados.gif (1285 bytes)
Actividades
No es posible disponer de lámparas que emitan a todas las frecuencias posibles, solamente existen lámparas hechas de materiales cuya emisión corresponde a unas determinadas líneas del espectro. Algunas de las líneas de emisión son muy débiles y otras son brillantes.
En las tablas que vienen a continuación se proporcionan los espectros de emisión de metales y gases. La longitud de onda se da en angstrom. Los números en negrita indican las líneas de mayor brillo.
Aluminio (arco) Cobre (arco en el vacío) Mercurio (lámpara de arco) Sodio (en llama) Cadmio (arco) Cinc (arco en el vacío)
3083
3093
3944
3962
4663
5057
5696
5723
3248
3274
4023
4063
5105
5153
5218
5700
5782
3126
3131
3650
4047
4358
4916
4960
5461
5770
5791
6152
6232
5890
5896
3261
3404
3466
3611
3982
4413
4678
4800
5086
5338
5379
6438
3036
3072
3345
4680
4722
4811
4912
4925
6103
6332
Argón Helio Hidrógeno Neón Nitrógeno Oxígeno
3949
4044
4159
4164
4182
4190
4191
4198
4201
4251
4259
4266
4272
4300
4334
4335
3889
4026
4221
5016
5876
6678
7065
4102
4340
4341
4861
6563
4538
4576
4704
4709
4715
4789
5331
5341
5358
5401
5853
5882
5965
6143
6266
6383
6402
6506
7174
7245
5754
5803
5853
5904
5957
6012
6068
6251
6321
6393
6467
6543
6622
6703
6787
5200
5300
5550
5640
Para realizar la práctica que simula el efecto fotoeléctrico se han de seguir los siguientes pasos:
Elegir el material de la placa metálica con el que experimentar el efecto fotoeléctrico, en el control selección titulado Cátodo.
Introducir la longitud de onda de la radiación que ilumina la placa, en angstrom (cuatro cifras) tomándola de las tablas anteriores.
Seleccionar la intensidad de la radiación un número mayor que cero, en el control de selección titulado Intensidad de la luz. Comprobar que cuando mayor sea la intensidad mayor es la desviación del amperímetro cuando pasa corriente por la fotocélula.
Pulsar en el botón titulado Fotón.
Si no hay emisión, introducir un valor menor de la longitud de onda (mayor frecuencia).
Si hay emisión, observar el movimiento del electrón. El campo eléctrico frena al electrón y eventualmente, le hace regresar a la placa metálica si su energía cinética no es suficiente.
Modificar el potencial variable de la batería, introduciendo otro valor en el control de edición titulado Diferencia de potencial, hasta conseguir que el electrón llegue justo a la placa opuesta, el amperímetro deja de marcar el paso de corriente, o empieza a marcar el paso de corriente.
Guardar el potencial de la batería bien por exceso o por defecto, y la longitud de onda en el control área de texto situada a la izquierda de la ventana, pulsando en el botón titulado Datos.
Repetir la experiencia introduciendo una nuevo valor para la longitud de onda de la radicación que ilumina la placa metálica.
Una vez que se han recolectado un número suficiente de datos (cuanto más mejor), se pulsa el botón titulado Enviar para representar gráficamente los datos en el applet situado más abajo.
Los pares de datos: longitud de onda, potencial de detención, se pueden introducir manualmente en dicha área de texto, separando cada par de datos mediante una coma, y pulsando la tecla Retorno o Enter.
Pulsar en el botón titulado Enviar para representar gráficamente los datos en el applet situado más abajo.
Resultados
Pulsar en el botón Calcular, para obtener la representación gráfica de los datos y la recta que mejor ajusta. Si el número de datos es insuficiente, o se ha producido algún error se pulsa en el botón Borrar, para limpiar el área de texto.
Se obtiene la energía de arranque de los electrones del metal leyendo la ordenada en el origen de la recta trazada, o el valor del parámetro b en la parte superior del applet.
La pendiente de la recta es el valor del parámetro a y mide el cociente entre las constantes fundamentales h/e según se ha explicado en la descripción.
Para obtener el valor de la constante h de Planck, se debe tener en cuenta que el eje horizontal es la frecuencia de la radiación electromagnética en unidades 1014 Hz. La carga del electrón es 1.6·10-19 C. Por tanto, el valor de h se obtiene multiplicando la pendiente a por la carga e y dividiendo por el factor 1014.
h=a·1.6 10-19 ·10-14 Js
Se aconseja al estudiante que haga por sí mismo el tratamiento de los datos de este ejemplo instructivo, representando gráficamente los datos experimentales y determinando la recta de regresión que mejor ajusta. Posteriormente, comparará sus resultados con los del programa interactivo. Los datos de la experiencia se pueden recoger en tablas como la siguiente:
METAL=
Longitud de onda Potencial V0
Energía de arranque f=
Constante de Planck h=
Elegir otro metal en el control selección titulado Cátodo, para experimentar otra vez el efecto fotoeléctrico, volviendo a obtener el valor de la constante h de Planck.
Teoría Cuántica de la Luz
Teoría fotónica o cuántica de la luz
Basándose en la hipótesis cuántica que M. Planck desarrolló en 1900 para la radiación térmica de los cuerpos negros, A. Einstein propuso en 1905 que en el efecto fotoeléctrico (efe), la radiación electromagnética interaccionaba con los electrones de igual forma.
Supuso que la energía luminosa tenía naturaleza discontinua, o sea estaba cuantizada.
Pero no sólo en el acto de la emisión o absorción como lo supuso Planck, sino que también en la propagación permanecía en pequeños paquetes, en especie de pequeños átomos de energía.
En su hipótesis, Einstein, imagina que la luz se propaga por el espacio, transportando la energía en gránulos o paquetes de luz.
Por tanto, la energía electromagnética que se propaga con ella está distribuida de forma discontinua, constando cada haz de luz de un número entero de paquetes de energía o cuantos, de valor:
E = h · f
En 1916, en su Teoría de la Relatividad General (TRG), Einstein demostró que estos cuantos de energía obedecen a la ecuación
E = p · c = m · c2
lo que implica la existencia real de dichos paquetes de energía.
Pasó a ser llamada Teoría de los Cuantos o Fotónica de la luz.
Y fue G.N. Lewis quién propuso llamarlos fotones, término que ya había sido utilizado por I. Newton en su teoría corpuscular de la luz. A modo de homenaje.
De esta forma, el efe vuelve a plantear el antiguo debate onda-corpúsculo para la luz, que hasta esos momentos estaba sin vencedor.
Para una magnífica simulación interactiva del efecto fotoeléctrico.
Espectro de los Elementos
Ya sabemos que cuando hacemos pasar la luz a través de un prisma óptico se produce el efecto llamado dispersión que consiste en la separación de las distintas longitudes de onda que forman el rayo incidente.
La luz blanca produce al descomponerla lo que llamamos un espectro continuo, que contiene el conjunto de colores que corresponde a la gama de longitudes de onda que la integran.
espectro solar
Sin embargo, los elementos químicos en estado gaseoso y sometidos a temperaturas elevadas producen espectros discontinuos en los que se aprecia un conjunto de líneas que corresponden a emisiones de sólo algunas longitudes de onda. El siguiente gráfico muestra el espectro de emisión del Na (sodio):
espectro emisión del sodio
El conjunto de líneas espectrales que se obtiene para un elemento concreto es siempre el mismo, incluso si el elemento forma parte de un compuesto complejo, y cada elemento produce su propio espectro diferente al de cualquier otro elemento. Esto significa que cada elemento tiene su propia firma espectral.
Si hacemos pasar la luz blanca por una sustancia antes de atravesar el prisma sólo pasarán aquellas longitudes de onda que no hayan sido absorbidas por dicha sustancia y obtendremos el espectro de absorción de dicha sustancia. El gráfico siguiente muestra el espectro de absorción del sodio:
espectro de absorción del sodio
Observa que el sodio absorbe las mismas longitudes de onda que es capaz de emitir.
La regularidad encontrada en los espectros discontinuos supone un apoyo muy importante para comprender la estructura de los átomos.
esquina inferior izquierda esquina inferior derecha
Espectro Electromagnético
Se denomina espectro electromagnético a la distribución energética del conjunto de las ondas electromagnéticas. Referido a un objeto se denomina espectro electromagnético o simplemente espectro a la radiación electromagnética que emite (espectro de emisión) o absorbe (espectro de absorción) una sustancia.
Peso Atómico Promedio ( uma)
El peso atómico (también llamado masa atómica relativa) (símbolo: A) es una cantidad física definida como la suma de la cantidad de las masas y del número atómico con el símbolo (Z) de un elemento (de un origen dado) expresado en unidades de masa atómica o U.M.A. (es decir, a 1/12 de la masa de un átomo de carbono-12).1 2 El concepto se utiliza generalmente sin mayor calificación para referirse al peso atómico estándar, que a intervalos regulares publica la International Union of Pure and Applied Chemistry (IUPAC).3 4 Se pretende que sean aplicables a materiales de laboratorios normales.
Los valores de estos pesos atómicos estándar están reimpresos en una amplia variedad de libros de texto, catálogos comerciales, pósters, etcétera. Para describir esta cantidad física se puede usar también la expresión «masa atómica relativa». Desde por lo menos 18605 y hasta la década de 1960, el uso continuado de la locución ha atraído una controversia considerable6 (véase más adelante).
A diferencia de las masas atómicas (las masas de los átomos individuales), los pesos atómicos no son constantes físicas. Varían de una muestra a otra. Sin embargo, en muestras «normales» son suficientemente constantes para ser de importancia fundamental en química. No se debe confundir al peso atómico con la masa molecular.
Isótopos
Se denomina isótopos a los átomos de un mismo elemento, cuyos núcleos tienen una cantidad diferente de neutrones, y por lo tanto, difieren en número másico.
Número Básico
En química, el número másico o número de masa es la suma del número de protones y el número de neutrones del núcleo de un átomo. Se simboliza con la letra A (el uso de esta letra proviene de alemán Atomgewicht, que quiere decir peso atomico, aunque sean conceptos distintos que no deben confundirse).
Número Atómico
El número atómico es el número de cargas positivas elementales, o protones, que transportan los núcleos de todos los isótopos de un elemento dado.
En un primer momento, el número atómico era el orden que se le daba a un elemento cuando se les ordenaba por orden creciente según sus masas atómicas.
En 1913, Johannes H. van den Broek, analizando toda la información conocida, descubrió que el número de cargas elementales del núcleo atómico era igual al número atómico. Más adelante, Niels Bohr adoptó este descubrimiento para desarrollar su teoría cuántica sobre la estructura de los átomos y el origen de los espectros.
Actualmente, Z es una cantidad nuclear conocida sin ningún error para todos los núcleos. No obstante, la carga efectiva Ze es conocida con sus errores experimentales correspondientes, como toda magnitud física.
El Núcleo Atómico
El Núcleo Atómico.
El núcleo atómico és la pequeña parte central del átomo, con carga eléctrica positiva y en la que se concentra la mayor parte de la masa del átomo. Las principales partículas subatómicas de los núcleos de los átomos són los protones y los neutrones o los nucleones (excepto el del hidrógeno ordinario o protio, que contiene únicamente un protón). Un mismo elemento químico está caracterizado por el el número de protones del núcleo que determina la carga positiva total. Éste número se denomina número atómico. El número másico es el total de protones y neutrones.
El núcleo atómico és la pequeña parte central del átomo, con carga eléctrica positiva y en la que se concentra la mayor parte de la masa del átomo. Las principales partículas subatómicas de los núcleos de los átomos són los protones y los neutrones o los nucleones (excepto el del hidrógeno ordinario o protio, que contiene únicamente un protón). Un mismo elemento químico está caracterizado por el el número de protones del núcleo que determina la carga positiva total. Éste número se denomina número atómico. El número másico es el total de protones y neutrones.
Dalton, Thomson, Rutherford
INTRODUCCIÓN
A finales del siglo XIX y principios del siglo XX, los estudios de los modelos atómicos han revolucionado la forma de entender el universo. Un nuevo mundo microscópico comenzó a desmoronarse.
La ciencia en general estaba recibiendo una herramienta muy poderosa que facilitaría la futura vida humana y también sirven como punto de partida para un nuevo mundo tecnológico que empezaba a tomar forma.
Hasta entonces, el precursor de este nuevo modelo aún permanecía aristotélicas y filósofos presocráticos ideas. Fue con Demócrito y Leucipo que vino la primera teoría sobre la naturaleza de la materia - atomismo. Más tarde se introdujo la teoría del flogisto - que era conocido como el espíritu ígneo = que desprendía las reacciones de combustión. Sin embargo, finalmente la punta con los datos experimentales. El misterio aún quedaba: que la materia estaba compuesta? surgen nuevas ideas.
MODELO DE ATÓMICA DE DALTON (1803)
Dalton modelo atómico
John Dalton
• El material se compone de átomos que no podrá ser dividido;
• Los átomos de un mismo elemento tienen los mismos elementos de masa y diferentes átomos químicos tienen diferentes masas;
• propuso inicialmente la idea de la reacción química: átomos de elementos diferentes se pueden combinar en diversas proporciones simple pero estas combinaciones químicas, cada átomo contiene su identidad;
modelo de átomo-Dalton
El modelo atómico de Dalton (bola de piscina)
• Propone la molécula idea inicial - compuestos químicos consisten en una combinación de dos o más elementos en una proporción fija.
La contribución de Dalton a la química era extremadamente importante, con sus ideas simples, pero crucial para la comprensión de las reacciones químicas y moléculas. Aunque esta propuesta de algunas formulaciones incorrectas, a continuación, dado nuevo impulso para futuras investigaciones en el mundo macroscópico podría explicarse por el mundo microscópico de los datos experimentales, junto con el razonamiento lógico. Su modelo cuenta con el átomo como una esfera masiva, invisible e indestructible e indivisible. Es el modelo atómico conocido como la "bola de billar".
modelo del pudín de ciruelo (1897)
Joseph John Thomson
Joseph John Thomson
La electricidad es un fenómeno que nos acompaña a diario. La atracción de la propiedad de los cuerpos se conoce desde la antigüedad. Nombre de la electricidad proviene de la palabra griega elektron = lo que atrae.
En 1833, el químico Inglés y físico Michael Faraday, llevaron a cabo una serie de experimentos de electrólisis (proceso de descomposición química de las sustancias mediante el paso de corriente eléctrica).
Observó que la masa depositada de una sustancia dada era proporcional a la cantidad de electricidad utilizada. En 1891, George Stoney propuso el nombre de electrones para la unidad natural de la electricidad en ese momento aún se desconoce, pero, como se ha demostrado por los datos experimentales.
Se sabía que se produce al pasar la electricidad a un gas rarificado atrapado en un tubo, un filamento cuyo color depende únicamente de la cantidad de corriente que pasa a través del tubo se emite. Además, la irradiación del electrodo negativo produce cuando la luz chocó con el otro extremo del tubo de vidrio.
Estos rayos producen sombras mientras caminaban recta. A medida que el electrodo negativo ya fue llamado cátodo, estos rayos fueron llamados "rayos catódicos".
El inglés William Crookes inventó la bombilla rayos catódicos consistían en un tubo de vidrio que tenía una bomba de vacío. Cuando el aire u otro gas sometido a baja presión y se sometió a alto voltaje, estos rayos dejando el ánodo y viajar hacia el cátodo. Crookes cree que estos rayos constituyen una corriente de moléculas.
Modelo atómico de Thomson
Modelo atómico de Thomson
El físico Inglés Joseph John Thomson realizó una serie de experimentos con la bombilla Crookes, probando el aire y luego otros tipos de gases. En una insertado dos polos (a = un imán de campo electromagnético) de la región de la ampolla que pasó los rayos catódicos y se encontró que estos rayos sufren cambios hacia el polo positivo, por lo que estos rayos eran naturaleza negativa.
En estos experimentos se determinó la relación entre la carga y la masa de los rayos de carga negativa. Se encontró que esta relación tenía siempre el mismo valor independientemente del material utilizado en los electrodos o de gas en el tubo. Estos resultados llevaron a la conclusión de Thomson que los rayos catódicos consistían en cargas eléctricas negativas realizadas por las partículas de la materia, estos rayos fueron llamadas electrones.
Thomson en 1897, propone que los electrones eran partes de átomos y redactaron el siguiente modelo: el átomo es un fluido de carga positiva en la que se incrusta electrones en una distribución uniforme de la carga. Por analogía, podemos imaginar un pan dulce con frutas confitadas en el que la masa de pan dulce serían los electrones de líquidos y fruta con incrustaciones de carga positiva.
Sin embargo, este modelo se conoce como el pudín de ciruela, pasas de uva, donde las incrustaciones representan los electrones y la masa del pastel que representaría la parte positiva.
Este modelo sirvió para confirmar definitivamente la idea de divisibilidad de la materia y su naturaleza eléctrica.
Modelo de Rutherford (1911)
Ernest Rutherford
Ernest Rutherford
El esfuerzo de muchos científicos en ese momento generó gran atención a cualquier fenómeno que apareció, por simple que era. Varias cosas sucedieron de forma natural y nuevos hallazgos parecen culminar en un nuevo modelo propuesto por Ernest Rutherford. Entre estos hechos, es posible enumerar:
• En 1895, el físico alemán Wilhelm Roentgem utilizando tubos de rayos catódicos descubrió los rayos X, los rayos mostró un tipo de radiación capaz de superar ciertos materiales e impresionar una placa fotográfica;
• En 1897, el físico francés, Antoine Henry Becquerel descubrió que el elemento uranio rayos que tenían la capacidad de pasar a través de objetos opacos emite.
• Pierre y Marie Curie aislaron otros elementos nuevos como el radio y el polonio, la misma propiedad, que fue nombrado radiactividad en 1898.
• Rutherford contribuye en un paso posterior que muestra una parte de la radiación de ciertos elementos radiactivos fueron cargados positivamente partículas que se mueven a gran velocidad y fueron llamados partículas alfa (α). Más tarde se demostró que estas partículas corresponden a núcleos de helio doblemente ionizados.
Rutherford se decantó por partículas alfa como proyectiles para bombardear hojas metálicas muy finas. Se utilizaron varios tipos diferentes de hojas de metal. Rigurosamente las partículas alfa no son visibles, pero generan un "flash" visibles cuando se golpea un mamparo cubierta con sulfuro de zinc. aparato de Rutherford consistió fragmento polonio (partícula alfa elemento emisor) y una placa de plomo de espesor que tiene un agujero, una hoja delgada de metal y una pantalla de cubierta con sulfuro de zinc. Se probaron varios tipos de metales, y el oro era el elemento que fue proporcionado por mejores observaciones. Los dos asistentes Rutherford, Geiger y Marsden montado el aparato y llevaron a cabo los primeros experimentos.
Se esperaba que mediante la colocación de una capa delgada de oro entre el conductor y la pantalla, las partículas alfa se cruzarían la hoja recta, el sufrimiento no es más que pequeñas desviaciones. Sin embargo, una pequeña fracción de estas partículas ha sufrido grandes cambios y algunos como estivem ricocheteadas. Sus asistentes escribieron: "Si tenemos en cuenta la masa de la partícula alfa y su gran velocidad (1,8 x 109 cm / seg) es, sin embargo, es sorprendente que algunos de ellos pueden convertirse en una capa de oro 6 x 10-5 cm en un ángulo de 90 ° o más ". Mediante el análisis de esta observación Rutherford dijo: "Es casi tan
Modelo atómico de Rutherford
Modelo atómico de Rutherford
increíble que disparamos una granada de 15 pulgadas contra una hoja de papel y nos devolvió el golpe ".
Para explicar las desviaciones con ángulos mayores de 90 ° o el hecho de que la partícula alfa rebotar Rutherford llegó a la conclusión de que ya no podía pensar en una distribución uniforme de la carga, conforme a lo dispuesto para el modelo atómico de Thomson. Por lo tanto, Rutherford propuso que las cargas atómicas se concentran en dos regiones distintas: una pequeña y densa, cargada positivamente centro, que fue llamado núcleo y los espacios vacíos de la región rodeada por los electrones que se llaman nube de electrones en movimiento. También ha demostrado que por cada 10.000 partículas alfa (diez mil) que pasan a través de la hoja en una línea recta fue desviado demostró que esta deducción el diámetro del átomo es de 10.000 a 100.000 veces mayor que su núcleo. Por analogía, se puede imaginar el estadio de fútbol Maracaná como el átomo: el núcleo sería el balón en el centro del césped y la nube de electrones sería el resto del estadio (de campo, gradas y aparcamiento).
Los resultados experimentales Rutherford concluyeron que:
• El átomo tiene espacio más vacío que lleno (lo que explica el hecho de que la mayoría de las partículas alfa pasan a través de la hoja de metal sin sufrir grandes desviaciones).
• La mayor parte del átomo de la masa se concentra en una pequeña región con carga positiva y el centro fue llamado el núcleo. Posteriormente estas cargas positivas serían llamados protones.
Este modelo fue satisfactoria para aclarar el fenómeno de dispersión de partículas alfa en una hoja de metal, pero el comportamiento de los electrones aún estaba por descifrar de una manera más clara. Según su modelo de Rutherford podría compararse con una pequeña sistema solar, en la que lo haría núcleo de papel del sol. Los electrones describen órbitas alrededor del núcleo que se mueve en los espacios vacíos en órbitas fijas, de tal manera que los planetas alrededor del sol.
Rutherford mismo reconoce un defecto en su analogía, no pudo explicar la estabilidad átomo, al considerar sólo la mecánica newtoniana. Una partícula cargada como el electrón para describir una órbita podría perder energía y caer en el núcleo. Este callejón sin salida comenzó a desmoronarse con el modelo de Bohr, como el siguiente.
Modelo de Bohr (1913)
Niels Henrik Bohr
Niels Henrik Bohr
A principios del siglo XX, el estudio de diversos fenómenos físicos activar fuertes debates entre los científicos para explicar fenómenos que tenían diferentes explicaciones para el mismo proceso.
Las pruebas experimentales y estudios teóricos han venido demostrando poco a poco que el universo electrónico fantástica de átomos, el comportamiento de las partículas sigue diferentes leyes de los aplicados a los cuerpos grandes.
En un intento de explicar la estabilidad del átomo con núcleo y electrones moviéndose alrededor de este núcleo, el danés Niels Henrik Bohr propuso los siguientes postulados (postulado = instrucción aceptada como verdadera sin pruebas):
• Los electrones describen órbitas circulares alrededor del núcleo, tales órbitas niveles o capas fueron nombrados;
• Cada uno de estos niveles tiene un cierto valor de la energía;
• Cuanto más lejos del núcleo más grande es el nivel de energía;
• No siga siendo el electrón entre dos niveles de energía;
• Los electrones tienen una energía cuantificada (paquetes con ciertos valores de energía). Por lo que no va a cambiar el nivel si se obtiene la energía correcta, exactamente igual a la diferencia de energía entre un nivel y otro.
• El electrón para recibir la energía (electricidad, luz, calor, etc.), se excita y saltando de un interno a una más externa y en su regreso al nivel anterior que emite parte de esta energía en forma de ondas electromagnéticas (luz visible , radiación ultravioleta, calor, etc.).
El modelo atómico de Bohr puede explicar eficazmente el espectro de hidrógeno, el ensayo a la llama y los fuegos artificiales (en este caso la energía de polvo es suficiente para excitar los electrones).
Bohr también llega a la conclusión de que la energía implicada en tales emisiones varía de átomo a átomo porque sus electrones ocupan diferentes niveles de energía que tienen diferentes frecuencias, pronto tener diferentes longitudes de onda, lo que resulta en la emisión de diferentes colores. En pocas palabras, tienen diferentes saltos cuánticos.
Toda la materia cuando se calienta a una temperatura suficientemente alta emite energía en forma de radiación (luz). Por ejemplo, si una persona hace que la luz de una lámpara de filamento incandescente común pasa a través de un prisma se descompone en varios colores como colores del arco iris. Esta descomposición se conoce como espectro de luz brillante
Modelo atómico de Bohr
Modelo atómico de Bohr
visible. Otro tipo de descomposición se produce cuando se pone un CD o DVD en la luz.
Bohr ha creado un aparato similar a un gas de hidrógeno atrapamiento tubo de rayos catódicos dentro de ella. Al calentar este tubo o haciendo pasar una chispa eléctrica a través de él, empezó a emitir luz.
Este tubo se colocó estratégicamente entre rendijas y un prisma. La luz se filtró y se refleja en una pantalla blanca y se verificó la presencia de líneas finas de diferentes colores - estas líneas fueron llamados espectro discontinuo del átomo de hidrógeno. Mediante la variación de la tensión en estas líneas espectrales de luz fueron más cerca entre sí hasta que una región continua aparecen como si se tratara de una mezcla de todos estos colores.
El avance de los estudios cuántica estableció que la presencia de un cierto número de electrones en cada nivel de energía sólo es posible. Como resultado de esta observación fue posible establecer el número máximo de electrones en cada uno de los niveles de energía o capa de electrones.
A finales del siglo XIX y principios del siglo XX, los estudios de los modelos atómicos han revolucionado la forma de entender el universo. Un nuevo mundo microscópico comenzó a desmoronarse.
La ciencia en general estaba recibiendo una herramienta muy poderosa que facilitaría la futura vida humana y también sirven como punto de partida para un nuevo mundo tecnológico que empezaba a tomar forma.
Hasta entonces, el precursor de este nuevo modelo aún permanecía aristotélicas y filósofos presocráticos ideas. Fue con Demócrito y Leucipo que vino la primera teoría sobre la naturaleza de la materia - atomismo. Más tarde se introdujo la teoría del flogisto - que era conocido como el espíritu ígneo = que desprendía las reacciones de combustión. Sin embargo, finalmente la punta con los datos experimentales. El misterio aún quedaba: que la materia estaba compuesta? surgen nuevas ideas.
MODELO DE ATÓMICA DE DALTON (1803)
Dalton modelo atómico
John Dalton
• El material se compone de átomos que no podrá ser dividido;
• Los átomos de un mismo elemento tienen los mismos elementos de masa y diferentes átomos químicos tienen diferentes masas;
• propuso inicialmente la idea de la reacción química: átomos de elementos diferentes se pueden combinar en diversas proporciones simple pero estas combinaciones químicas, cada átomo contiene su identidad;
modelo de átomo-Dalton
El modelo atómico de Dalton (bola de piscina)
• Propone la molécula idea inicial - compuestos químicos consisten en una combinación de dos o más elementos en una proporción fija.
La contribución de Dalton a la química era extremadamente importante, con sus ideas simples, pero crucial para la comprensión de las reacciones químicas y moléculas. Aunque esta propuesta de algunas formulaciones incorrectas, a continuación, dado nuevo impulso para futuras investigaciones en el mundo macroscópico podría explicarse por el mundo microscópico de los datos experimentales, junto con el razonamiento lógico. Su modelo cuenta con el átomo como una esfera masiva, invisible e indestructible e indivisible. Es el modelo atómico conocido como la "bola de billar".
modelo del pudín de ciruelo (1897)
Joseph John Thomson
Joseph John Thomson
La electricidad es un fenómeno que nos acompaña a diario. La atracción de la propiedad de los cuerpos se conoce desde la antigüedad. Nombre de la electricidad proviene de la palabra griega elektron = lo que atrae.
En 1833, el químico Inglés y físico Michael Faraday, llevaron a cabo una serie de experimentos de electrólisis (proceso de descomposición química de las sustancias mediante el paso de corriente eléctrica).
Observó que la masa depositada de una sustancia dada era proporcional a la cantidad de electricidad utilizada. En 1891, George Stoney propuso el nombre de electrones para la unidad natural de la electricidad en ese momento aún se desconoce, pero, como se ha demostrado por los datos experimentales.
Se sabía que se produce al pasar la electricidad a un gas rarificado atrapado en un tubo, un filamento cuyo color depende únicamente de la cantidad de corriente que pasa a través del tubo se emite. Además, la irradiación del electrodo negativo produce cuando la luz chocó con el otro extremo del tubo de vidrio.
Estos rayos producen sombras mientras caminaban recta. A medida que el electrodo negativo ya fue llamado cátodo, estos rayos fueron llamados "rayos catódicos".
El inglés William Crookes inventó la bombilla rayos catódicos consistían en un tubo de vidrio que tenía una bomba de vacío. Cuando el aire u otro gas sometido a baja presión y se sometió a alto voltaje, estos rayos dejando el ánodo y viajar hacia el cátodo. Crookes cree que estos rayos constituyen una corriente de moléculas.
Modelo atómico de Thomson
Modelo atómico de Thomson
El físico Inglés Joseph John Thomson realizó una serie de experimentos con la bombilla Crookes, probando el aire y luego otros tipos de gases. En una insertado dos polos (a = un imán de campo electromagnético) de la región de la ampolla que pasó los rayos catódicos y se encontró que estos rayos sufren cambios hacia el polo positivo, por lo que estos rayos eran naturaleza negativa.
En estos experimentos se determinó la relación entre la carga y la masa de los rayos de carga negativa. Se encontró que esta relación tenía siempre el mismo valor independientemente del material utilizado en los electrodos o de gas en el tubo. Estos resultados llevaron a la conclusión de Thomson que los rayos catódicos consistían en cargas eléctricas negativas realizadas por las partículas de la materia, estos rayos fueron llamadas electrones.
Thomson en 1897, propone que los electrones eran partes de átomos y redactaron el siguiente modelo: el átomo es un fluido de carga positiva en la que se incrusta electrones en una distribución uniforme de la carga. Por analogía, podemos imaginar un pan dulce con frutas confitadas en el que la masa de pan dulce serían los electrones de líquidos y fruta con incrustaciones de carga positiva.
Sin embargo, este modelo se conoce como el pudín de ciruela, pasas de uva, donde las incrustaciones representan los electrones y la masa del pastel que representaría la parte positiva.
Este modelo sirvió para confirmar definitivamente la idea de divisibilidad de la materia y su naturaleza eléctrica.
Modelo de Rutherford (1911)
Ernest Rutherford
Ernest Rutherford
El esfuerzo de muchos científicos en ese momento generó gran atención a cualquier fenómeno que apareció, por simple que era. Varias cosas sucedieron de forma natural y nuevos hallazgos parecen culminar en un nuevo modelo propuesto por Ernest Rutherford. Entre estos hechos, es posible enumerar:
• En 1895, el físico alemán Wilhelm Roentgem utilizando tubos de rayos catódicos descubrió los rayos X, los rayos mostró un tipo de radiación capaz de superar ciertos materiales e impresionar una placa fotográfica;
• En 1897, el físico francés, Antoine Henry Becquerel descubrió que el elemento uranio rayos que tenían la capacidad de pasar a través de objetos opacos emite.
• Pierre y Marie Curie aislaron otros elementos nuevos como el radio y el polonio, la misma propiedad, que fue nombrado radiactividad en 1898.
• Rutherford contribuye en un paso posterior que muestra una parte de la radiación de ciertos elementos radiactivos fueron cargados positivamente partículas que se mueven a gran velocidad y fueron llamados partículas alfa (α). Más tarde se demostró que estas partículas corresponden a núcleos de helio doblemente ionizados.
Rutherford se decantó por partículas alfa como proyectiles para bombardear hojas metálicas muy finas. Se utilizaron varios tipos diferentes de hojas de metal. Rigurosamente las partículas alfa no son visibles, pero generan un "flash" visibles cuando se golpea un mamparo cubierta con sulfuro de zinc. aparato de Rutherford consistió fragmento polonio (partícula alfa elemento emisor) y una placa de plomo de espesor que tiene un agujero, una hoja delgada de metal y una pantalla de cubierta con sulfuro de zinc. Se probaron varios tipos de metales, y el oro era el elemento que fue proporcionado por mejores observaciones. Los dos asistentes Rutherford, Geiger y Marsden montado el aparato y llevaron a cabo los primeros experimentos.
Se esperaba que mediante la colocación de una capa delgada de oro entre el conductor y la pantalla, las partículas alfa se cruzarían la hoja recta, el sufrimiento no es más que pequeñas desviaciones. Sin embargo, una pequeña fracción de estas partículas ha sufrido grandes cambios y algunos como estivem ricocheteadas. Sus asistentes escribieron: "Si tenemos en cuenta la masa de la partícula alfa y su gran velocidad (1,8 x 109 cm / seg) es, sin embargo, es sorprendente que algunos de ellos pueden convertirse en una capa de oro 6 x 10-5 cm en un ángulo de 90 ° o más ". Mediante el análisis de esta observación Rutherford dijo: "Es casi tan
Modelo atómico de Rutherford
Modelo atómico de Rutherford
increíble que disparamos una granada de 15 pulgadas contra una hoja de papel y nos devolvió el golpe ".
Para explicar las desviaciones con ángulos mayores de 90 ° o el hecho de que la partícula alfa rebotar Rutherford llegó a la conclusión de que ya no podía pensar en una distribución uniforme de la carga, conforme a lo dispuesto para el modelo atómico de Thomson. Por lo tanto, Rutherford propuso que las cargas atómicas se concentran en dos regiones distintas: una pequeña y densa, cargada positivamente centro, que fue llamado núcleo y los espacios vacíos de la región rodeada por los electrones que se llaman nube de electrones en movimiento. También ha demostrado que por cada 10.000 partículas alfa (diez mil) que pasan a través de la hoja en una línea recta fue desviado demostró que esta deducción el diámetro del átomo es de 10.000 a 100.000 veces mayor que su núcleo. Por analogía, se puede imaginar el estadio de fútbol Maracaná como el átomo: el núcleo sería el balón en el centro del césped y la nube de electrones sería el resto del estadio (de campo, gradas y aparcamiento).
Los resultados experimentales Rutherford concluyeron que:
• El átomo tiene espacio más vacío que lleno (lo que explica el hecho de que la mayoría de las partículas alfa pasan a través de la hoja de metal sin sufrir grandes desviaciones).
• La mayor parte del átomo de la masa se concentra en una pequeña región con carga positiva y el centro fue llamado el núcleo. Posteriormente estas cargas positivas serían llamados protones.
Este modelo fue satisfactoria para aclarar el fenómeno de dispersión de partículas alfa en una hoja de metal, pero el comportamiento de los electrones aún estaba por descifrar de una manera más clara. Según su modelo de Rutherford podría compararse con una pequeña sistema solar, en la que lo haría núcleo de papel del sol. Los electrones describen órbitas alrededor del núcleo que se mueve en los espacios vacíos en órbitas fijas, de tal manera que los planetas alrededor del sol.
Rutherford mismo reconoce un defecto en su analogía, no pudo explicar la estabilidad átomo, al considerar sólo la mecánica newtoniana. Una partícula cargada como el electrón para describir una órbita podría perder energía y caer en el núcleo. Este callejón sin salida comenzó a desmoronarse con el modelo de Bohr, como el siguiente.
Modelo de Bohr (1913)
Niels Henrik Bohr
Niels Henrik Bohr
A principios del siglo XX, el estudio de diversos fenómenos físicos activar fuertes debates entre los científicos para explicar fenómenos que tenían diferentes explicaciones para el mismo proceso.
Las pruebas experimentales y estudios teóricos han venido demostrando poco a poco que el universo electrónico fantástica de átomos, el comportamiento de las partículas sigue diferentes leyes de los aplicados a los cuerpos grandes.
En un intento de explicar la estabilidad del átomo con núcleo y electrones moviéndose alrededor de este núcleo, el danés Niels Henrik Bohr propuso los siguientes postulados (postulado = instrucción aceptada como verdadera sin pruebas):
• Los electrones describen órbitas circulares alrededor del núcleo, tales órbitas niveles o capas fueron nombrados;
• Cada uno de estos niveles tiene un cierto valor de la energía;
• Cuanto más lejos del núcleo más grande es el nivel de energía;
• No siga siendo el electrón entre dos niveles de energía;
• Los electrones tienen una energía cuantificada (paquetes con ciertos valores de energía). Por lo que no va a cambiar el nivel si se obtiene la energía correcta, exactamente igual a la diferencia de energía entre un nivel y otro.
• El electrón para recibir la energía (electricidad, luz, calor, etc.), se excita y saltando de un interno a una más externa y en su regreso al nivel anterior que emite parte de esta energía en forma de ondas electromagnéticas (luz visible , radiación ultravioleta, calor, etc.).
El modelo atómico de Bohr puede explicar eficazmente el espectro de hidrógeno, el ensayo a la llama y los fuegos artificiales (en este caso la energía de polvo es suficiente para excitar los electrones).
Bohr también llega a la conclusión de que la energía implicada en tales emisiones varía de átomo a átomo porque sus electrones ocupan diferentes niveles de energía que tienen diferentes frecuencias, pronto tener diferentes longitudes de onda, lo que resulta en la emisión de diferentes colores. En pocas palabras, tienen diferentes saltos cuánticos.
Toda la materia cuando se calienta a una temperatura suficientemente alta emite energía en forma de radiación (luz). Por ejemplo, si una persona hace que la luz de una lámpara de filamento incandescente común pasa a través de un prisma se descompone en varios colores como colores del arco iris. Esta descomposición se conoce como espectro de luz brillante
Modelo atómico de Bohr
Modelo atómico de Bohr
visible. Otro tipo de descomposición se produce cuando se pone un CD o DVD en la luz.
Bohr ha creado un aparato similar a un gas de hidrógeno atrapamiento tubo de rayos catódicos dentro de ella. Al calentar este tubo o haciendo pasar una chispa eléctrica a través de él, empezó a emitir luz.
Este tubo se colocó estratégicamente entre rendijas y un prisma. La luz se filtró y se refleja en una pantalla blanca y se verificó la presencia de líneas finas de diferentes colores - estas líneas fueron llamados espectro discontinuo del átomo de hidrógeno. Mediante la variación de la tensión en estas líneas espectrales de luz fueron más cerca entre sí hasta que una región continua aparecen como si se tratara de una mezcla de todos estos colores.
El avance de los estudios cuántica estableció que la presencia de un cierto número de electrones en cada nivel de energía sólo es posible. Como resultado de esta observación fue posible establecer el número máximo de electrones en cada uno de los niveles de energía o capa de electrones.
Breves notas sobre las evidencias experimentales del Electrón , Protón y Neutron
Breves notas sobre las evidencias experimentales del Electrón , Protón y Neutron.
Quark - Wikipedia, la enciclopedia libre https://es.wikipedia.org/wiki/Quark En física de partículas, los cuarks o quarks, junto con los leptones, son los constituyentes ... 5 Subestructura; 6 Véase también; 7 Notas; 8 Enlaces externos ... Se habían descubierto los quarks de manera experimental lo que permitió obtener el .... de los quarks en un protón se corresponde exactamente a la del electrón, un ... Átomo - Wikipedia, la enciclopedia libre https://es.wikipedia.org/wiki/Átomo Un átomo es la unidad constituyente más pequeña de la materia que tiene las propiedades de ... Los electrones de un átomo son atraídos por los protones en un núcleo atómico por ... Los protones y los neutrones en el núcleo son atraídos el uno al otro por una fuerza diferente, ... 6 Véase también; 7 Notas y referencias. Electrones,Protones y Neutrones - Taringa! www.taringa.net › Ciencia y educación 15 abr. 2012 - Desde el punto de vista físico, el electrón tiene una carga eléctrica de igual magnitud, pero de ... Por esto se dice que los protones y electrones tienen cargas de +1 y -1 .... Distintos montajes experimentales buscaron estas hipotéticas ... cuya vida media es extremadamente breve (véase Radiactividad). Un nuevo modelo atómico (2da parte) (página 2) - Monografias.com www.monografias.com › Fisica El Neutrón es en realidad una partícula combinada: Protón y Electrón, en este caso ... de nuevas partículas, lógicamente en forma teórica primero y experimental luego, las ... El electrón solo puede conjugar un sector de su anillo con el Protón. ..... como evidencia para confirmar las teorías presentadas del Electrón Anular y ... III. EL MODELO ESTÁNDAR www.cubaeduca.cu/medias/cienciatodos/Libros_3/ciencia3/.../sec_7.htm 14 [Nota 14] ... Salvo el electrón y el protón, todas las partículas de la materia son inestables. ... extremadamente breves, que se miden en millonésimas de segundos. ... Hasta la fecha, se han encontrado evidencias experimentales de la ... Bosón de Higgs: qué es y por qué es tan importante - La Voz de Galicia www.lavozdegalicia.es › Sociedad 6 jul. 2012 - Guía para entender la importancia de la partícula que explicaría el origen de la masa. ... Los componentes del átomo (electrones, protones y neutrones) son ... que indican la probabilidad de que un resultado experimental se deba a la ... Otras evidencias indirectas observadas en procesos físicos que ... I. ¿QUÉ SON LAS CARGAS? bibliotecadigital.ilce.edu.mx/sites/ciencia/volumen1/.../44/.../sec_3.html El protón tiene la misma cantidad de carga que el electrón pero positiva. ... No existe evidencia experimental de que se haya medido una partícula con una .... Otros datos similares se encuentran en el libro Breve compendio de la sphera y de ... Niveles de energía atómicos, ¿cómo sabemos que están ahí ... https://cuentos-cuanticos.com/2011/10/25/niveles-de-energia-atomicos/ 25 oct. 2011 - Para ello haremos una breve discusión del modelo atómico de Bohr y ... evidencias experimentales de los niveles atómicos de los átomos. ... Un electrón puede pasar de un nivel de energía E_{inicial} ... estemos trabajando (el número de protones del núcleo) y la energía está medida en electronVoltios. [PDF]11. EL SPIN www.lfp.uba.ar/.../notas%20de%20cursos/notasmecanicacuantica/11Spin... protones y neutrones no están completamente descriptas por el modelo de masa .... En breve tiempo Uhlenbeck y Goudsmit (y otros como Wolfgang Pauli, ... Además, la evidencia experimental más reciente tiende a indicar que el electrón es ..
Quark - Wikipedia, la enciclopedia libre https://es.wikipedia.org/wiki/Quark En física de partículas, los cuarks o quarks, junto con los leptones, son los constituyentes ... 5 Subestructura; 6 Véase también; 7 Notas; 8 Enlaces externos ... Se habían descubierto los quarks de manera experimental lo que permitió obtener el .... de los quarks en un protón se corresponde exactamente a la del electrón, un ... Átomo - Wikipedia, la enciclopedia libre https://es.wikipedia.org/wiki/Átomo Un átomo es la unidad constituyente más pequeña de la materia que tiene las propiedades de ... Los electrones de un átomo son atraídos por los protones en un núcleo atómico por ... Los protones y los neutrones en el núcleo son atraídos el uno al otro por una fuerza diferente, ... 6 Véase también; 7 Notas y referencias. Electrones,Protones y Neutrones - Taringa! www.taringa.net › Ciencia y educación 15 abr. 2012 - Desde el punto de vista físico, el electrón tiene una carga eléctrica de igual magnitud, pero de ... Por esto se dice que los protones y electrones tienen cargas de +1 y -1 .... Distintos montajes experimentales buscaron estas hipotéticas ... cuya vida media es extremadamente breve (véase Radiactividad). Un nuevo modelo atómico (2da parte) (página 2) - Monografias.com www.monografias.com › Fisica El Neutrón es en realidad una partícula combinada: Protón y Electrón, en este caso ... de nuevas partículas, lógicamente en forma teórica primero y experimental luego, las ... El electrón solo puede conjugar un sector de su anillo con el Protón. ..... como evidencia para confirmar las teorías presentadas del Electrón Anular y ... III. EL MODELO ESTÁNDAR www.cubaeduca.cu/medias/cienciatodos/Libros_3/ciencia3/.../sec_7.htm 14 [Nota 14] ... Salvo el electrón y el protón, todas las partículas de la materia son inestables. ... extremadamente breves, que se miden en millonésimas de segundos. ... Hasta la fecha, se han encontrado evidencias experimentales de la ... Bosón de Higgs: qué es y por qué es tan importante - La Voz de Galicia www.lavozdegalicia.es › Sociedad 6 jul. 2012 - Guía para entender la importancia de la partícula que explicaría el origen de la masa. ... Los componentes del átomo (electrones, protones y neutrones) son ... que indican la probabilidad de que un resultado experimental se deba a la ... Otras evidencias indirectas observadas en procesos físicos que ... I. ¿QUÉ SON LAS CARGAS? bibliotecadigital.ilce.edu.mx/sites/ciencia/volumen1/.../44/.../sec_3.html El protón tiene la misma cantidad de carga que el electrón pero positiva. ... No existe evidencia experimental de que se haya medido una partícula con una .... Otros datos similares se encuentran en el libro Breve compendio de la sphera y de ... Niveles de energía atómicos, ¿cómo sabemos que están ahí ... https://cuentos-cuanticos.com/2011/10/25/niveles-de-energia-atomicos/ 25 oct. 2011 - Para ello haremos una breve discusión del modelo atómico de Bohr y ... evidencias experimentales de los niveles atómicos de los átomos. ... Un electrón puede pasar de un nivel de energía E_{inicial} ... estemos trabajando (el número de protones del núcleo) y la energía está medida en electronVoltios. [PDF]11. EL SPIN www.lfp.uba.ar/.../notas%20de%20cursos/notasmecanicacuantica/11Spin... protones y neutrones no están completamente descriptas por el modelo de masa .... En breve tiempo Uhlenbeck y Goudsmit (y otros como Wolfgang Pauli, ... Además, la evidencia experimental más reciente tiende a indicar que el electrón es ..
Partículas Fundamentales del Átomo
Partículas fundamentales del átomo.
1º- El protón de carga positiva y una masa de 1,672 × 10–27 Kg o, en relación al electrón, unas 1836 veces la masa de un electrón. se encuentra en el núcleo del átomo. 938,3 MeV/c2.
2º- El neutrón, con carga neutra y una masa de 1,674 × 10–27 Kg o, en relación al electrón, unas 1836 veces la masa de un electrón. se encuentra en el núcleo del átomo. 939,2 MeV/c2.
3º- El electrón con carga negativa y fuera del núcleo del átomo, el electrón posee una masa de 9,1×10−31 Kg. 0,5 MeV/c2.
Teoría Atómica de Dalton

Teoría atómica de Dalton.
 Las leyes ponderales de las combinaciones químicas encontraron una explicación satisfactoria en la teoría atómica formulada por DALTON en 1803 y publicada en 1808.Dalton reinterpreta las leyes ponderales basándose en el concepto de átomo. Establece los siguientespostulados o hipótesis, partiendo de la idea de que la materia es discontinua:
Las leyes ponderales de las combinaciones químicas encontraron una explicación satisfactoria en la teoría atómica formulada por DALTON en 1803 y publicada en 1808.Dalton reinterpreta las leyes ponderales basándose en el concepto de átomo. Establece los siguientespostulados o hipótesis, partiendo de la idea de que la materia es discontinua:
Los elementos están constituidos por átomos consistentes en partículas materiales separadas e indestructibles;
Los átomos de un mismo elemento son iguales en masa y en todas las demás cualidades.
Los átomos de los distintos elementos tienen diferentes masa y propiedades
Los compuestos se forman por la unión de átomos de los correspondientes elementos en una relación numérica sencilla. Los «átomos» de un determinado compuesto son a su vez idénticos en masa y en todas sus otras propiedades.
Aunque el químico irlandés HIGGINS, en 1789, había sido el primero en aplicar la hipótesis atómica a las reacciones químicas, es Dalton quien le comunica una base más sólida al asociar a los átomos la idea de masa.
Los átomos de DALTON difieren de los átomos imaginados por los filósofos griegos, los cuales los suponían formados por la misma materia primordial aunque difiriendo en forma y tamaño. La hipótesis atómica de los antiguos era una doctrina filosófica aceptada en sus especulaciones científicas por hombres como GALILEO, BOYLE, NEWTON, etc., pero no fue hasta DALTON en que constituye una verdadera teoría científica mediante la cual podían explicarse y coordinarse cuantitativamente los fenómenos observados y las leyes de las combinaciones químicas.
La teoría atómica constituyó tan sólo inicialmente una hipótesis de trabajo, muy fecunda en el desarrollo posterior de la Química, pues no fue hasta finales del siglo XIX en que fue universalmente aceptada al conocerse pruebas físicas concluyentes de la existencia real de los átomos. Pero fue entonces cuando se llegó a la conclusión de que los átomos eran entidades complejas formadas por partículas más sencillas y que los átomos de un mismo elemento tenían en muchísimos casos masa distinta. Estas modificaciones sorprendentes de las ideas de DALTON acerca de la naturaleza de los átomos no invalidan en el campo de la Química los resultados brillantes de la teoría atómica.
Justificación de las leyes ponderales.
Las suposiciones de DALTON permiten explicar fácilmente las leyes ponderales de las combinaciones químicas, ya que la composición en peso de un determinado compuesto viene determinada por el número y peso de los átomos elementales que integran el «átomo» del compuesto.
Ley de la conservación de la materia.
Por ser los átomos indivisibles e indestructibles los cambios químicos han de consistir únicamente en un reagrupamiento de átomos y, por tanto, no puede haber en el mismo variación alguna de masa al no variar el número de átomos presentes.
Ley de las proporciones definidas.
Si se combinan n átomos del elemento A con m átomos del elemento B y los pesos respectivos de estos átomos sona y b
Ley de las proporciones múltiples.
Si dos elementos se unen en varias proporciones para formar distintos compuestos quiere decir que sus átomos se unen en relaciones numéricas diferentes. Si un átomo del elemento A se une, por ejemplo, con uno y con dos átomos del elemento B, se comprende que la relación en peso de las cantidades de este elemento (uno y dos átomos) que se unen con una misma cantidad de aquél (un átomo) estén en relación de 1 : 2. Si los átomos de los elementos A y B se unen en otras cualesquiera relaciones numéricas, siempre de números enteros sencillos, se encontrará igualmente una relación sencilla entre las cantidades de uno de los elementos que se unen con una cantidad determinada del otro elemento.
Ley de las proporciones recíprocas.
Si suponemos que los elementos se uniesen siempre en la relación atómica 1 : 1, la ley de las proporciones recíprocas no sólo sería evidente sino que los pesos de combinación serían a su vez los pesos atómicos. Aunque los elementos se unen en relaciones atómicas diferentes, 1 : 2, 1 : 3, 2 : 3 etcétera, puede fácilmente calcularse que las cantidades en peso de distintos elementos que se unen con una cantidad fija de un elemento dado han de estar en relación sencilla con sus respectivos pesos atómicos y que dichas cantidades, multiplicadas necesariamente en todo caso por números enteros sencillos, han de ser las que se combinen entre sí en las correspondientes combinaciones mutuas.
Fracaso ante la ley de Gay-Lussac.
Para DALTON las últimas partículas de los elementos gaseosos como el hidrógeno, oxígeno, cloro, etc., eran necesariamente simples y estaban constituidas por un solo átomo (así, H, O, CI, N, ...) y que las de compuestos gaseosos tan corrientes como el agua o el cloruro de hidrógeno eran naturalmente compuestas pero formadas por sólo dos átomos distintos (HO, CIH, ... ). Sin embargo, con estas fórmulas no se podían explicar las relaciones volumétricas de Gay-Lussac:
 La conclusión experimental de GAY-LUSSAC de que un volumen de cloro se une con un volumen de hidrógeno para dar lugar a dos volúmenes de cloruro de hidrógeno llevó a DALTON a suponer que en los volúmenes iguales de cloro y de hidrógeno debían existir igual número de átomos.
La conclusión experimental de GAY-LUSSAC de que un volumen de cloro se une con un volumen de hidrógeno para dar lugar a dos volúmenes de cloruro de hidrógeno llevó a DALTON a suponer que en los volúmenes iguales de cloro y de hidrógeno debían existir igual número de átomos.
Al imaginar que estos elementos se unen átomo a átomo, formarán un mismo número de «átomos» (hoy moléculas) de cloruro de hidrógeno, al ser estos«átomos» indivisibles, debían ocupar, en cambio, un volumen doble según los resultados de Gay Lussac.
La hipótesis de que en volúmenes iguales de gases debían existir igual número de «átomos» tuvo DALTON que descartarla llegando a la conclusión de que los resultados de GAY-LUSSAC eran inexactos. comenta
Por el contrario, si la ley de Gay-Lussac era cierta estaba en contradicción con los postulados de DALTON y su teoría atómica.
Átomo
Un átomo es la unidad constituyente más pequeña de la materia que tiene las propiedades de un elemento químico. Cada sólido, líquido, gas y plasma se compone de átomos neutros o ionizados.
Naturaleza Eléctrica de la Materia
1. La estructura de la materia
La materia es todo aquello que tiene masa y que, por lo tanto, ocupa un volumen.
Desde hace muchos años, una de las grandes preocupaciones de los científicos ha sido poder conocer la constitución de la materia para poder llegar a predecir su comportamiento.
Los avances experimentales y teóricos del siglo XX han permitido conocer mejor la estructura interna de la materia. Ahora sabemos que toda materia está formada por un conjunto de átomos que, a su vez, están constituidos por las llamadas partículas subatómicas: los electrones, los protones y los neutrones (principalmente).
En los átomos que forman la materia se pueden distinguir dos partes:
El núcleo, que es la parte central del átomo y que ocupa una parte muy pequeña. En su interior se encuentran los protones y los neutrones, entre otras partículas subátomicas.
La corteza, que es la parte exterior del átomo y ocupa la mayor parte de su volumen. Esta parte está formada por un único tipo de partículas subatómicas, los electrones que se mueven a una gran velocidad alrededor del núcleo, describiendo unas trayectorias elípticas llamadas órbitas.
estructura materia
Estructura de la materia
2. La carga eléctrica
Los protones (partículas que forman parte del núcleo del átomo) y electrones (que rodean el núcleo del átomo) crean fuerzas de atracción y de repulsión debido a que estas partículas atómicas tienen una carga eléctrica.
Se puede establecer una ley muy sencilla en relación a las fuerzas de atracción y repulsión entre partículas: las cargas de diferente símbolo se atraen y las del mismo signo se repelen.
La carga de un protón es la misma que la de un electrón, con la diferencia de que la carga de protones es positiva y la de los electrones negativa.
En cambio, los neutrones no tienen carga eléctrica, ni positiva ni negativa. Por lo tanto los neutrones no son atraídos ni repelidos por los protones ni los electrones.
La carga eléctrica es una propiedad general de la materia que se puede medir, cuya unidad es el Coulomb (C).
La masa y la carga eléctrica de las principales partículas subatómicas son:
Masa (Kg) Carga (C)
Protón (p) 1,6725 • 10-27 1,6 • 10 -19
Neutrón (n) 1,6748 • 10-27 -
Electrón (e) 9,1095 • 10-31 1,6 • 10 -19
3. El campo eléctrico
El campo eléctrico es el espacio alredededor de una carga eléctrica. En él se manifiestan las fuerzas de atracción o de repulsión sobre otras cargas eléctricas situadas en este espacio.
4. Pérdida o ganancia de electrones
En relación a la naturaleza eléctrica del átomo, hay que destacar que la carga eléctrica de un átomo es nula porque tiene el mismo número de protones que de electrones, teniendo así la misma cantidad de cargas positivas que negativas.
Hay, sin embargo, excepciones que hay que tener en cuenta:
En algunas situaciones los átomos pueden perder o ganar electrones y quedar cargados eléctricamente. Estos átomos se llaman iones.
Cuando un átomo pierde uno o diversos electrones queda cargado positivamente y recibe el nombre de catión.
De forma contraria, cuando un átomo gana uno o varios electrones queda cargado negativamente, recibiendo el nombre de anión.
5. ¿De dónde viene la electricidad?
La energía eléctrica o electricidad es un fenómeno físico que se origina a raíz de las cargas eléctricas y de la interacción entre ellas. Así, son los electrones y los protones las dos partículas subatómicas principales que pueden originar la aparición de energía eléctrica.
La electricidad se puede originar o transmitir provocando el movimiento de cargas eléctricas de un punto a otro.
Esta situacion es muy común ya en la propia Naturaleza, dado que la energía eléctrica se manifiesta de diversas formas, transformándose en otros tipos de energía. Ejemplos de este fenómeno son las tormentas eléctricas o el sistema nervioso de los seres vivos.
En el siguiente enlace puedes conocer una serie de magnitudes eléctricas que ayudan a definir las características de la electricidad.
La rama que estudia la interacción de las cargas eléctricas cuando estas están en reposo se denomina electrostática.
6. Materiales conductores y materiales aislantes
Las cargas eléctricas se pueden mover a través de los materiales, per no se mueven de la misma manera en todos ellos. A la propiedad que indica la facilidad con que las cargas se mueven a a través de un material específico se la denomina conductividad.
Según su conductividad, podemos dividir todos los materiales en dos grandes grupos:
Materiales conductores. Son los que tienen una estructura atómica que favorece que las cargas eléctricas se puedan mover con facilidad por su interior. En general, todos los metales son buenos conductores.
Materiales aislantes, son los que tienen los electrones muy ligados al átomo al que pertenecen, de manera que no se pueden mover con facilidad. Algunos ejemplos aislantes son la madera, la resina o el cristal.
¿Deseas saber más sobre la conductividad eléctrica? Tienes un juego a tu disposición.
7. La corriente eléctrica
La corriente eléctrica es el movimiento de los electrones por un conductor. Este movimiento de cargas eléctricas se puede comparar con el agua del río, y de la misma manera que podemos medir el caudal de un río en un punto podemos medir la intensidad de la corriente eléctrica.
Para que el movimiento de electrones se produzca hace falta que entre los extremos del conductor haya una diferencia de potencial , que también se llama tensión o voltaje.
8. Tipos de corriente eléctrica
El movimiento de electrones (cargas negativas) del generador se produce desde su polo positivo (lugar de salida de los electrones) hasta su polo negativo (lugar donde vuelven los electrones). Cuando dicho flujo es al revés (de polo negativo a positivo), se considera que la corriente es negativa. Asi, y dependiendo del sentido del movimiento de dichos electrones, se puede clasificar la corriente eléctrica en:
Corriente continua , que se caracteriza porque los electrones se mueven en un solo sentido por el hilo conductor. Ejemplos de generadores de corriente continua son las pilas o las dinamos.
Corriente alterna, cuya característica principal es que los polos del generador cambian de negativo a positivo en el mismo periodo, provocando que el flujo de electrones no mantengan el mismo sentido. La generacion de este tipo de corriente la realizan los alternadores.
En el siguiente juego puedes saber más acerca ed la corriente continua y la corriente alterna.
Clasificación de la Materia

CLASIFICACIÓN DE LA MATERIA
|  |
La materia la podemos encontrar en la naturaleza en forma de sustancias puras y de mezclas.
* Las sustancias puras son aquéllas cuya naturaleza y composición no varían sea cual sea su estado. Se dividen en dos grandes grupos: Elementos y Compuestos.
- Elementos: Son sustancias puras que no pueden descomponerse en otras sustancias puras más sencillas por ningún procedimiento. Ejemplo: Todos los elementos de la tabla periódica: Oxígeno, hierro, carbono, sodio, cloro, cobre, etc. Se representan mediante su símbolo químico y se conocen 115 en la actualidad.

- Compuestos: Son sustancias puras que están constituidas por 2 ó más elementos combinados en proporciones fijas. Los compuestos se pueden descomponer mediante procedimientos químicos en los elementos que los constituyen. Ejemplo: Agua, de fórmula H2O, está constituida por los elementos hidrógeno (H) y oxígeno (O) y se puede descomponer en ellos mediante la acción de una corriente eléctrica (electrólisis). Los compuestos se representan mediante fórmulas químicas en las que se especifican los elementos que forman el compuesto y el número de átomos de cada uno de ellos que compone la molécula. Ejemplo: En el agua hay 2 átomos del elemento hidrógeno y 1 átomo del elemento oxígeno formando la molécula H2O.
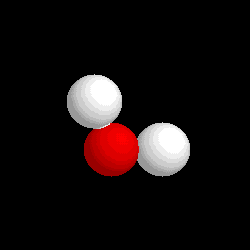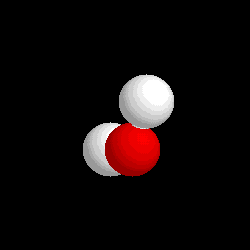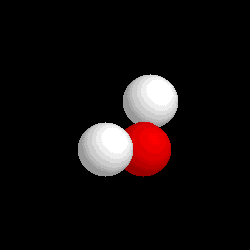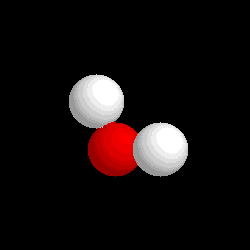 |
Molécula de agua (H2O), formada por 2 átomos de hidrógeno (blancos) y 1 átomo de oxígeno (rojo)
|
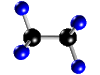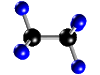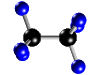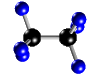 |
Molécula de etano (C2H6), formada por 2 átomos de carbono (negros) y 6 átomos de hidrógeno (azul)
|
 |
Molécula de butano (C4H10), formada por 4 átomos de carbono (negros) y 10 átomos de hidrógeno (blancos)
|
Cuando una sustancia pura está formada por un solo tipo de elemento, se dice que es una sustancia simple. Esto ocurre cuando la molécula contiene varios átomos pero todos son del mismo elemento.Ejemplo: Oxígeno gaseoso (O2), ozono (O3), etc. Están constituidas sus moléculas por varios átomos del elemento oxígeno.

* Las mezclas se encuentran formadas por 2 ó más sustancias puras. Su composición es variable. Se distinguen dos grandes grupos: Mezclas homogéneas y Mezclas heterogéneas.
- Mezclas homogéneas: También llamadas Disoluciones. Son mezclas en las que no se pueden distinguir sus componentes a simple vista. Ejemplo: Disolución de sal en agua, el aire, una aleación de oro y cobre, etc.

- Mezclas heterogéneas: Son mezclas en las que se pueden distinguir a los componentes a simple vista.Ejemplo: Agua con aceite, granito, arena en agua, etc.
 |  |
 |
En esta página encontrarás más información sobre elementos, compuestos y mezclas.
En esta página encontrarás un esquema sobre lo visto anteriormente y una actividad para practicar.
Realiza las siguientes actividades.
Los procedimientos físicos más empleados para separar los componentes de una mezcla heterogénea son: la filtración, la decantación y la separación magnética. Estos métodos de separación son bastante sencillos por el hecho de que en estas mezclas se distinguen muy bien los componentes.
- Filtración: Este procedimiento se emplea para separar un líquido de un sólido insoluble. Ejemplo: Separación de agua con arena. A través de materiales porosos como el papel filtro, algodón o arena se puede separar un sólido que se encuentra suspendido en un líquido. Estos materiales permiten solamente el paso del líquido reteniendo el sólido.
 |  |
- Decantación: Esta técnica se emplea para separar 2 líquidos no miscibles entre sí. Ejemplo: Agua y aceite. La decantación se basa en la diferencia de densidad entre los dos componentes, que hace que dejados en reposo, ambos se separen hasta situarse el más denso en la parte inferior del envase que los contiene. De esta forma, podemos vaciar el contenido por arriba (si queremos tomar el componente menos denso) o por abajo (si queremos tomar el más denso).
En la separación de dos líquidos no miscibles, como el agua y el aceite, se utiliza un embudo de decantación que consiste en un recipiente transparente provisto de una llave en su parte inferior. Al abrir la llave, pasa primero el líquido de mayor densidad y cuando éste se ha agotado se impide el paso del otro líquido cerrando la llave. La superficie de separación entre ambos líquidos se observa en el tubo estrecho de goteo.
 |  |  |  |

- Separación magnética: Esta técnica sirve para separar sustancias magnéticas de otras que no lo son. Al aproximar a la mezcla el imán, éste atrae a las limaduras de hierro, que se separan así del resto de la mezcla.
 |  |
En esta página puedes ver ejemplos de separaciones de mezclas heterogéneas.
Realiza las siguientes actividades.
Una disolución es una mezcla homogénea formada por 2 ó más sustancias puras en proporción variable. Las disoluciones pueden ser binarias (2 componentes), ternarias (3 componentes), etc. Ejemplo: Una mezcla de agua con sal es una disolución.
El componente de la disolución que se encuentra en mayor cantidad se llama disolvente y el o los que aparecen en menor cantidad se llaman solutos. Ejemplo: En una disolución de sal en agua, la sal es el soluto y el agua es el disolvente.
Las disoluciones binarias se clasifican según el estado de agregación en que se encuentran soluto y disolvente. en el siguiente cuadro podemos verlo:
| SOLUTO | DISOLVENTE | DISOLUCIÓN | EJEMPLO |
| GAS | GAS | GAS | AIRE  |
| LÍQUIDO | NIEBLA | ||
| SÓLIDO | POLVO EN EL AIRE | ||
| GAS | LÍQUIDO | LÍQUIDO | AMONIACO COMERCIAL |
| LÍQUIDO | ALCOHOL Y AGUA | ||
| SÓLIDO | SAL Y AGUA | ||
| GAS | SÓLIDO | SÓLIDO | HIDRÓGENO EN PALADIO |
| LÍQUIDO | AMALGAMAS (MERCURIO Y METAL) | ||
| SÓLIDO | ACERO INOXIDABLE |
3.1.- Concentración de una disolución
Las disoluciones pueden clasificarse en concentradas o diluidas según la cantidad de soluto sea grande o pequeña con respecto a la cantidad de disolvente. Pero estos términos son cualitativos, no dan una cantidad exacta medible. Para ello, se emplea el término concentración.
La concentración de una disolución es la cantidad de soluto que hay disuelto en una determinada cantidad de disolvente o en una determinada cantidad de disolución.
Existen distintas formas de expresar la concentración de una disolución:
1) Tanto por ciento en masa
Es la masa de soluto (en gramos) que hay en 100 gramos de disolución.
% en masa del soluto = (masa de soluto / masa de disolución) x 100
Ejemplo: Preparamos una disolución que contiene 2 g de cloruro de sodio (NaCl) y 3 g de cloruro de potasio (KCl) en 100 g de agua destilada. Calcula el tanto por ciento en masa de cada soluto en la disolución obtenida.
Primeramente, se trata de identificar a los solutos y al disolvente. En este caso, el disolvente es el agua, pues es la sustancia que se encuentra en mayor proporción y los solutos serán NaCl y KCl. La masa de soluto será la que hay para cada uno de ellos; la masa de disolución es la suma de todas las masas de sustancias presentes en la mezcla: 2 g + 3 g + 100 g = 105 g. Por tanto:
% en masa de NaCl = (2 g / 105 g) · 100 = 1,9 % de NaCl en la disolución.
% en masa de KCl = (3 g / 105 g) · 100 = 2,8 % de KCl en la disolución.
Esto indica que si tuviésemos 100 g de disolución, 1,9 g serían de cloruro sódico, 2,8 g serían de cloruro potásico y el resto, hasta 100 g, serían de agua.
2) Tanto por ciento en volumen
Es el volumen de soluto que hay en 100 volúmenes de disolución.
% en volumen del soluto = (volumen de soluto / volumen de disolución) x 100
Ejemplo: Preparamos una disolución añadiendo 5 ml de alcohol etílico junto a 245 ml de agua. Calcula el % en volumen de soluto en la disolución.
En este caso, el soluto es el alcohol pues está en menor cantidad y el disolvente es el agua. El volumen de disolución es la suma de volúmenes de los componentes (no tiene porqué ser así siempre): 5 ml + 245 ml = 250 ml. Por tanto:
% en volumen de alcohol = (5 ml / 250 ml) · 100 = 2 % de alcohol en la disolución.
3) Concentración en masa
Es la masa de soluto que hay disuelta por cada unidad de volumen de disolución.
Concentración en masa = masa de soluto / volumen de disolución
La unidad de concentración en masa, en el S.I., es el kg/m3 pero en la práctica se emplea el g/l.
Ejemplo: Preparamos una disolución añadiendo 20 g de sal a agua destilada hasta tener un volumen de 500 ml. Calcular la concentración en masa.
En este caso, el soluto es la sal y el disolvente es el agua. El volumen de disolución es 500 ml = 0,5 litros. Por tanto:
Concentración en masa = 20 g / 0,5 l = 40 g/l.
Realiza las siguientes actividades.
La cantidad de soluto que se puede disolver en una cantidad determinada de un disolvente es limitada. El azúcar, por ejemplo, es soluble en agua, pero si en un vaso de agua añadimos cada vez más y más azúcar, llegará un momento en el que ésta ya no se disuelva más y se deposite en el fondo. Además, se disuelve más cantidad de azúcar en agua caliente que en agua fría.
La cantidad máxima (en gramos) de cualquier soluto que se puede disolver en 100 g de un disolvente a una temperatura dada se denomina solubilidad de ese soluto a esa temperatura. Así, la solubilidad se expresa en gramos de soluto por 100 g de disolvente.
La solubilidad de una sustancia pura en un determinado disolvente y a una temperatura dada es otra de sus propiedades características.
Cuando una disolución contiene la máxima cantidad posible de soluto disuelto a una temperatura dada, decimos que está saturada a esa temperatura. En este caso, si añadimos más soluto, éste se quedará sin disolver.
4.1.- La solubilidad de los gases
Cuando se eleva la temperatura de una disolución de un gas en un líquido, se observa, por lo común, que le gas se desprende. Esto se produce porque la solubilidad de los gases en los líquidos disminuye al aumentar la temperatura. Ejemplo: Una bebida carbónica a temperatura ambiente tiene menos gas disuelto que si está fría, esto se debe a que a mayor temperatura se disuelve menos cantidad de gas y parte de éste se escapa.
4.2.- Curvas de solubilidad
En general, la solubilidad de una sustancia en un determinado disolvente aumenta a medida que se eleva la temperatura. Si se recoge en el laboratorio la cantidad de una sal, por ejemplo nitrato de potasio, que se disuelven en 100 g de agua a diferentes temperaturas obtenemos los siguientes datos:
| Temperatura | 20 ºC | 30 ºC | 40 ºC | 50 ºC | 60 ºC |
| Masa disuelta en 100 g de agua | 30 | 44 | 60 | 80 | 104 |
Al representar estos datos gráficamente se obtienen unas gráficas llamadas Curvas de solubilidad.

En esta gráfica se encuentran las curvas de solubilidad para diversas sales.
Realiza las siguientes actividades.
Existen varios métodos para separar los componentes de una mezcla homogénea o disolución. Entre los más utilizados están la cristalización y la destilación simple.
- Cristalización: Esta técnica consiste en hacer que cristalice un soluto sólido con objeto de separarlo del disolvente en el que está disuelto. Para ello es conveniente evaporar parte del disolvente o dejar que el proceso ocurra a temperatura ambiente. Si el enfriamiento es rápido se obtienen cristales pequeños y si es lento se formarán cristales de mayor tamaño.

- Destilación simple: Esta técnica se emplea para separar líquidos de una disolución en función de sus diferentes puntos de ebullición. Es el caso, por ejemplo, de una disolución de dos componentes, uno de los cuáles es volátil (es decir, pasa fácilmente al estado gaseoso). Cuando se hace hervir la disolución contenida en el matraz, el disolvente volátil, que tiene un punto de ebullición menor, se evapora y deja un residuo de soluto no volátil. Para recoger el disolvente así evaporado se hace pasar por un condensador por el que circula agua fría. Ahí se condensa el vapor, que cae en un vaso o en un erlenmeyer.
Ejemplo: Esta técnica se emplea para separar mezclas de agua y alcohol. El alcohol es más volátil que el agua y es la primera sustancia en hervir, enfriándose después y separándose así del agua.

Suscribirse a:
Comentarios (Atom)
